|
|
 行動遺伝生理学研究室
(東京都医学総合研究所)
行動遺伝生理学研究室
(東京都医学総合研究所)
|
本研究室では、ショウジョウバエの得意分野である多数の突然変異体や遺伝子組換え体を用いて、学習や記憶にどのような遺伝子やタンパクが関わっているのかを研究しています。さらに、学習や記憶は誰しも年齢と共に低下していくごく一般的に起こる生理的な変化ですが、この原因となる遺伝子の同定も目指して研究を行っています。学習記憶などを含めた脳の研究は今後も、ますます盛んになると考えられ、世界中の数多くの研究室が学習や記憶の機構を解明すべく鎬を削っています。
|
|
記憶回路動作機構の分子生理学的解析
|
|

ティーチングマシーン
記憶情報は動物全体にとって個体生存や種の保存に必要であり、人にあっては高度な精神活動や個性の表出を担う。記憶情報は精緻な、グリアを含めた神経回路(記憶回路)の働きによるものである。では記憶はどのように作られ、記憶回路は各種疾患や加齢、さらには生理状況に応じてどのような影響を受けるのか?記憶機構の本質を明らかにするには、記憶回路の神経活動に加えて、動作原理を裏打ちする分子・遺伝子の働きも含めた解析が重要である。このためには出来るだけ単純な神経回路を持つモデル動物で同定された記憶回路の挙動と記憶行動を結びつけて調べることが有用である。我々は右図ティーチングマシーンを利用した匂い条件付けを行動指標に、ショウジョウバエ微小脳で学習記憶に関与する遺伝子や神経回路を同定している。匂い条件付けでは入力した感覚情報に罰・報酬といった意味が付加されることで記憶情報が生成される。脳機能イメージングや電気化学的検出法を駆使して、記憶情報が生まれる過程、保持、読み出される過程を記憶回路の挙動として可視化すると共に、各種学習記憶関連遺伝子がこれら記憶回路の動作機序の制御にどのように関わっているのかを解明する。
|
|
|
|
|
後シナプス誘導性(オンデマンド)シナプス伝達機構の解明
|
|
学習記憶や精神活動に重要な働きを持つドーパミン(DA)やセロトニン(5HT)などのモノアミンやアセチルコリン(ACh)といった神経機能修飾因子は、神経は終末が高度に分枝し数多くの標的細胞に投射する神経細胞から放出される。教科書に記載されたシナプス伝達によれば神経伝達物質はシナプス前神経の活動に応じて起こるとある。ではこの様式に従って神経修飾因子も神経活動に応じて要・不要に関わらず全ての標的細胞に伝達物質を放出するのだろうか?我々はDAの放出がシナプス前神経細胞でなく、DAを必要とするシナプス後細胞により限局的に誘導される新たなシナプス伝達機構を見出した。そこでどのような分子機構や生理機構によりシナプス後細胞の活動が前終末からのDA放出を誘導するのか?さらにこうした後シナプス誘導性(オンデマンド)シナプス伝達機構が他の神経修飾因子の放出にも当てはまるのか?哺乳類にも保存されているのか?などを明らかにしていく。
|
|
|
加齢に伴う記憶低下機構の解明
|
|
我々は歳をとると電話番号や長い文章を覚えることが不得手になり、覚えていたことを思い出すことが難しくなる。こうした加齢に伴う記憶力低下(加齢性記憶障害)は恐らく記憶力を持つ全ての動物に起こる生物学的現象であるがその仕組みは多くが不明である。我々はショウジョウバエの寿命が1-2ヶ月と短いことを利用して加齢性記憶障害の分子遺伝学的解析を行い、加齢性記憶障害は単なる神経細胞の脱落などによる非特異的な障害で無く、中期記憶と呼ばれる特定の記憶過程や長期記憶機構の障害に起因すること、単一の遺伝子変異により、これら加齢性記憶障害が有意に抑制できることなどを見出した。ではどのような遺伝子が、どこで働くことにより加齢性記憶障害が起こるのか?より詳細な分子遺伝学的解析やプロテオミクスなどの生化学的手法と脳機能イメージングを組み合わせることで加齢性記憶障害の発現を裏打ちする分子機構や細胞生理機構を解明する。
|
|
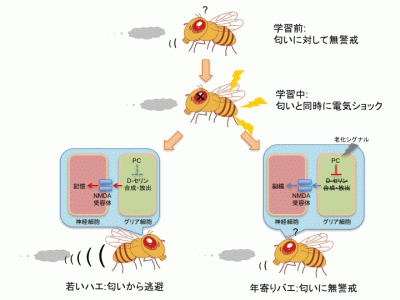
新たに見出されたグリア細胞による加齢性記憶障害機構
|
|
|
|
最近の研究業績
|
|
- Ueno K*, Suzuki E, Naganos S, Ofusa K, Horiuchi J, Saitoe M*. (2017). Coincident postsynaptic activity gates presynaptic dopamine release to induce plasticity in Drosophila mushroom bodies. eLife, 6, e21076.
- Hirano Y, Ihara K, Masuda T, Yamamoto T, Iwata I, Takahashi A, Awata H, Nakamura N, Takakura M, Suzuki Y, Horiuchi J, Okuno H, Saitoe M*. (2016). Shifting transcriptional machinery is required for long-term memory maintenance and modification in Drosophila mushroom bodies. Nat Commun. 7, 13471.
- Naganos S, Ueno K, Horiuchi J, Saitoe M*. (2016). Learning defects in Drosophila growth restricted chico mutants are caused by attenuated adenylyl cyclase activity. Mol Brain 9, 37.
- Matsuno M, Horiuchi J, Yuasa Y, Ofusa K, Miyashita T, Masuda T, Saitoe M*. (2015). Long-term memory formation in Drosophila requires training-dependent glial transcription. J Neurosci 35, 5557-5565. Picked up in “This week in the Journal”.
- Yamazaki D, Horiuchi J, Ueno K, Ueno T, Saeki S, Matsuno M, Naganos S, Miyashita T, Hirano Y, Nishikawa H, Taoka M, Yamauchi, Y, Isobe T, Honda Y, Kodama T, Masuda T, Saitoe M*. (2014). Glial dysfunction causes age-related memory impairment in Drosophila. Neuron 84, 753-763. Previewed in Neuron
- Saitoe M, Saeki S, Hirano Y, Horiuchi J. Age-related memory impairment in Drosophila. Behavioral Genetics of the Fly. 177-182. (Cambridge Univ press). 2014.
- Hirano Y, Saitoe M. (2013). Hunger and memory; CRTC coordinates long-term memory with the physiological state, hunger. Commun Integr Biol. 6, e25152.
- Hirano Y, Masuda T, Naganos S, Matsuno M, Ueno K, Miyashita T, Horiuchi J, Saitoe M. (2013). Fasting Launches CRTC to Facilitate Long-term Memory Formation in Drosophila. Science 339, 443-446.
- Ueno K, Naganos S, Hirano Y, Horiuchi J, Saitoe M. (2013). Long-term enhancement of synaptic transmission between antennal lobe and mushroom body in cultured Drosophila brain. J Physiol 591, 287-302. Featured in Perspectives
- Miyashita T, Oda Y, Horiuchi J, Yin JC, Morimoto T, Saitoe M. (2012). Mg2+ block of Drosophila NMDA receptors is required for long-term memory formation and CREB-dependent gene expression. Neuron 74, 887-898. Featured in Preview
|
|
|